| |
|
|
| |
Blitze unter Wasser |
|
|
|
|
| |
Versuch
Nr.031
Bewertung / Schwierigkeitsgrad:   
Zeitaufwand: ca. 15 Minuten |
|
|
|

|
| |
|
|
| |
Ziel:
Blitze unter Wasser??? Wie soll denn das gehen? .....eigentlich
unmöglich, mit ein paar Tricks aber doch! Mit relativ geringem
Aufwand und mit wenigen Chemikalien kann auch der Laie kleine Blitzerscheinungen
in einer Flüssigkeit erzeugen.
|
|
| |
Geräte:
Reagenzglas, Becherglas, Reagenzglashalterung, Einmalpipetten,
Spatel (Löffel)
|
|
| |
Chemikalien:
konzentrierter Schwefelsäure, Ethanol (Brennspiritus), Kaliumpermanganat
|
|
| |
Sicherheitshinweise:
Achtung: Auf
keinen Fall zu viel Kaliumpermanganat auf einmal in das Reagenzglas
werfen, da sonst eine zu heftige Reaktion einsetzen kann und die
Reaktionsmischung herausgeschleudert wird!
konz. Schwefelsäure (H2SO4):
C R 14-35-37 S26-30-36/37/39
Ethanol (C2H5OH): F
R11 S7-16
Kaliumpermanganat (KMnO4): O, Xn,
N R 8-22-50/53 S 60-61
Mangandioxid
(MnO2):Xn
R20/22-36 S25
 F F Xn Xn O O N N C C
|
|
| |
Einverständniserklärung:
Hiermit erklären Sie sich bereit den folgenden Versuch unter
eigener Verantwortung
und nur mit ausreichendem chemischen Wissen und geeigneten Schutzvorrichtungen
durchzuführen!
Der Autor kann für jegliche Personen- und Sachschäden
durch mögliche Fehlversuche nicht haftbar gemacht werden. (siehe
Sicherheitscheck bzw. Disclaimer) |
|
| |
|
|
| |
Versuchsanleitung: 
Ein trockenes, sauberes Reagenzglas wird der Sicherheit
wegen in eine Halterung eingespannt oder in einen Reagenzglashalter
gestellt. Danach füllt man es ca. 2 cm hoch mit konzentrierter
Schwefelsäure. Am besten benutzt man eine Pipette und verwendet
Schutzhandschuhe (Verätzungsgefahr!). Anschließend lässt
man vorsichtig eine 4 cm hohe Schicht Ethanol (oder Brennspiritus)
auf die Schwefelsäure fließen. Dabei darauf achten, dass
sich die beiden Flüssigkeiten nicht vermischen, d.h. am besten
benutzt man wieder eine Pipette und hält diese ca.1 cm über
dem Flüssigkeitsspiegel.
Nun
wirft man kleine Kaliumpermanganat-Kristalle in das Reagenzglas
und beobachtet ein Absinken bis zur Schwefelsäureschicht. Dort
treten rasch grüne, lila und braune Schlieren auf, begleitet
von kleinen Bläschen, die nach oben aufsteigen. Mit andauender
Reaktion bzw. bei neuer Zugabe von Kaliumpermanganat wird die Lösung
immer trüber.
 .
.  .
. 
Nach
kurzer Zeit, wenn vermehrt Gasblasen aufsteigen, kommt es an der
Grenzfläche zwischen Säure und Ethanol immer wieder zu
blitzartigen Entladungen, begleitet von kleinen Knallgeräuschen.
Die Funkenerscheinung dauert einige Minuten an, ehe sie nachlässt
und man wieder neue Kristalle nachwerfen kann (je nach Stärke
der Reaktion, kann die Zugabe beschleunigt bzw. verringert werden).

mit freundlichem Dank
an Volker
Piper vom Helmholtz-Gymnasium in Essen
|
|
| |
Entsorgung:
(siehe auch Entsorgungsmaßnahmen)
Nach beendeter Reaktion lässt man das Gemisch abkühlen
und zieht mit einer Pipette die obere organische Ethanolphase ab.
In einem kleinen Becherglas kann nun der Ethanol verdunsten.
Die verunreinigte Schwefelsäure-Phase wird mit Wasser (evtl.
Eis) verdünnt und mit Lauge neutralisiert. Die Entsorgung erfolgt
in den wässrigen Schwermetallabfällen.
|
|
| |
Erklärung
/ Hintergrund:
Da konz. Schwefelsäure eine Dichte von ca. 1.8 g
cm-3 und Brennspiritus
eine Dichte von ca. 0.8 g
cm-3 hat,
bleiben die beiden Flüssigkeiten längere Zeit voneinander
getrennt.
Lässt man konzentrierte
Schwefelsäure längere Zeit auf Kaliumpermanganat einwirken,
so entsteht Dimanganheptoxid Mn2O7.
Es ist ein hochexplosives Öl, das molekular aufgebaut ist und
aus zwei eckenverknüpften-MnO4-Tetraedern
besteht.
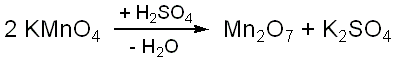
Es
ist allerdings sehr unbeständig und zerfällt gemäß
folgender Gleichung zu Braunstein (daher die Braunfärbung in
der Phasengrenzzone) und Sauerstoff.
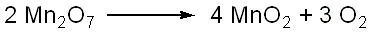
Der
freigesetzte Sauerstoff oxidiert nun an der Grenzfläche beider
Flüssigkeiten den Brennspiritus unter leichten Funkenerscheinungen
zu Kohlendioxid CO2 und Wasser H2O.
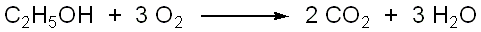
Was
die verschiedenen Farben während der Reaktion angeht, so ist
dies mit dem Durchlaufen der verschiedenen Oxidationsstufen des
Mangans zu erklären. Näheres hierzu beim Versuch "Mineralisches
Chamäleon" von A.Schunk.
|
|
| |
Links:
Blitze-Bildergallerie
1: tolle Seite mit vielen Bildern von verschiedensten Blitzarten.
Blitze-Bildergallerie
2: wolkenatlas.de mit vielen Aufnahmen der Wolken- und Wetterfotografie
Blitze
in Gewittern: Wie entstehen Blitze...die physikalische Entstehung
kostenloser
BLITZ-SPION: BLIDS - der Blitz-Informations-Dienst von Siemens
zeigt eine Übersicht über das aktuelle Gewittergeschehen
mit allen Blitzen in Deutschland, der Schweiz, Tschechien und Polen.
Blitzschutzbau
"Rhein-Main": 50 Fragen und Antworten rund um Blitze!
Entsorgung
von Mangansalzabfällen: Braunstein
Oxidationsstufen
des Mangans: Alles über die verschiedenen Oxidationsstufen
sowie deren Auftreten in der Praxis
Chemikalien-Lexikon
--- Kaliumpermanganat: Alles über Kaliumpermanganat
|
|