| |
|
|
| |
Silberspiegel - Tollens Reagenz |
|
|
|
|
|
|
|
|
| |
|
|
| |
Ziel:
Und wieder einmal gibt es einen Klassiker der Experimentierkunst,
den schon Justus von Liebig vor über 150 Jahren vorführte.
Er entwickelte den Silberspiegel, der den bis dahin gebräuchlichen
Quecksilberspiegel ersetzte, dessen Herstellung zum Siechtum und
qualvollen Tod vieler Arbeiter führte.
Im vorgestellten Experiment ist es möglich auf einfache und
schnelle Art und Weise Glaskugeln, Kolben oder Reagenzgläser
mit einer silbernen Schicht zu überziehen.
|
|
| |
Geräte:
Reagenzglas (Kolben oder anderes Glasgefäß),
Bunsenbrenner, Pasteurpipetten, Spatel, Schutzbrille
|
|
| |
Chemikalien:
Silbernitrat, gesättigte Glucoselösung (Traubenzucker),
Natriumhydroxid-Plätzchen, 2N wässrige Ammoniaklösung
|
|
| |
Sicherheitshinweise:
Natriumhydroxid (NaOH):
C R35 S26-36/37/39-45
Silbernitrat (AgNO3): C,N R
34-50/53 S 26-50-60-61
Ammoniak-Lösung
(NH3): C,N
R 34-50 S 26-36/37/39-45-61
 C C
 N N
|
|
| |
Einverständniserklärung:
Hiermit erklären Sie sich bereit den folgenden Versuch unter
eigener Verantwortung
und nur mit ausreichendem chemischen Wissen und geeigneten Schutzvorrichtungen
durchzuführen!
Der Autor kann für jegliche Personen- und Sachschäden
durch mögliche Fehlversuche nicht haftbar gemacht werden. (siehe
Sicherheitscheck bzw. Disclaimer) |
|
| |
|
|
| |
Versuchsanleitung: 
In ein völlig sauberes Reagenzglas (oder anderes
Glasgefäß) gibt man 5 ml Silbernitratlösung (0,1
molar, d.h. 17 g Silbernitrat gelöst in 1 l destilliertes Wasser
bzw. 0,85g in 50 ml dest. Wasser). Die Silbernitratlösung sollte
immer frisch hergestellt werden. Die Lösung wird nun mit soviel
Ammoniak-Lösung versetzt bis sich der dabei entstehende milchig
weise Niederschlag (Silberoxid) wieder auflöst.
Anschließend gibt man ein Natriumhydroxid-Plätzchen und
etwas gesättigte Glucoselösung (ca. 3 ml; Traubenzucker
solange in dest. Wasser auflösen bis ein Niederschlag zurück
bleibt) hinzu. Nun beginnt man sofort das Reagenzglas oder den Kolben
unter leichtem Erhitzen mit dem Bunsenbrenner kräftig zu schütteln.
Nach und nach scheidet sich an der Innenwand des Glases ein silberner
Überzug ab.
 Versuchsverlauf
in Bildern:
Versuchsverlauf
in Bildern: |
|
|
| |
Entsorgung:
(siehe auch Entsorgungsmaßnahmen)
Die übrigen Lösungen werden vorsichtig angesäuert
(z.B. mit Salpetersäure) und anschließend in die schwermetallhaltigen
Abfälle entsorgt.
|
|
| |
Erklärung
/ Hintergrund:
Silbernitrat zerfällt in wässriger Lösung vollständig
in seine Ionen.
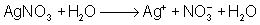
Ammoniak-Lösung
wirkt alkalisch, sodass die Silberionen mit den Hydroxidionen Silberoxid
bilden, was schwer löslich ist und als Niederschlag ausfällt.
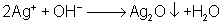
Dieser
Niederschlag kann dann mit weiterer Ammoniak-Lösung
in einem Silberdiamin-Komplex gebunden werden, der wiederum in Lösung
geht.
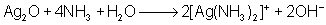
Die
zugegebene Glucose (der Traubenzucker) reduziert anschließend
die Ionen zu metallischem Silber, das sich an der Innenwand des
Glasgefäßes absetzen kann. Die Glucose selbst wird zur
Gluconsäure oxidiert.
Diese
hergestellte Mischung aus Ammoniak-Lösung, Natriumhydroxid
und Silbernitrat wird auch als Tollens Reagenz
bezeichent. Es dient allgemein dazu reduzierende Aldehyde zur entsprechenden
Carbonsäure zu oxidieren und damit indirekt mit dem Silberspiegel
nachzuweisen.
Allgemeine
Gesamtreaktion:
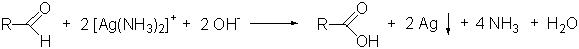
|
|
| |
Links:
Liebig-Jahr
2003: Seite zum 200. Geburtstag Justus Liebigs
Justus
Liebig - Leben und Werk: Seite des Liebig Museums Gießen
Zuckerchemie:
Informationen und Experimente rund um verschiedene Zucker
Quellenangabe:
[1] By Terabyte at de.wikipedia [GFDL (www.gnu.org/copyleft/fdl.html) or CC-BY-SA-3.0 (www.creativecommons.org/licenses/by-sa/3.0/)], from Wikimedia Commons |
|