| |
|
|
| |
Die
magische Farbwechsel-Spritze |
|
|
|
|
|
|
|
|
| |
|
|
| |
Ziel:
Scheinbar wie von Zauberhand verändert sich die
Farbe einer Lösung in einer Spritze wenn man diese aufzieht.
Nachdem man den Kolben zurückfährt, stellt sich wieder
die ursprüngliche Farbe ein. Dieser Vorgang ist beliebig oft
wiederholbar!
Es erfolgt keine Zugabe von Chemikalien, die Temperatur wird nicht
verändert,.... was ist also des Rätsels Lösung? Die
Erklärung ist verblüffend einfach und wird Laien sowie
gestandene Chemiker beeindrucken.
|
|
| |
Geräte:
Plastikspritze, Becherglas, Pinzette
|
|
| |
Chemikalien:
Indikator (Bromthymolblau), Trockeneis (CO2), Wasser
|
|
| |
Sicherheitshinweise:
Bromthymolblau
(3',3"-Dibromthymolsulfonphthalein, C27H28Br2O5S):
geringe Gefährlichkeit
Trockeneis
(CO2): VORSICHT! Sehr tiefe
Temperaturen! Erfrierungsgefahr!
|
|
| |
Einverständniserklärung:
Hiermit erklären Sie sich bereit den folgenden Versuch unter
eigener Verantwortung
und nur mit ausreichendem chemischen Wissen und geeigneten Schutzvorrichtungen
durchzuführen!
Der Autor kann für jegliche Personen- und Sachschäden
durch mögliche Fehlversuche nicht haftbar gemacht werden. (siehe
Sicherheitscheck bzw. Disclaimer) |
|
| |
|
|
| |
Versuchsanleitung: 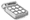
Vorbereitung:
Man fülle Leitungswasser in ein Becherglas und füge ein
paar Tropfen Bromthymolblau hinzu. Das Wasser färbt sich dunkelgrün.
Nun gibt man kleine Stückchen Trockeneis hinein, wartet bis
es abreagiert hat und zieht die Lösung mit einer Plastikspritze
auf. (Die Lösung sollte einen merklichen Farbunterschied zur
der Lösung vor der Trockeneis-Behandlung aufweisen. Die grün-blaue
Farbe geht ins Gelbliche über. Am einfachsten ist dies indem
man einen Teil der ursprünglichen Lösung zum Vergleich
aufhebt.)
Nun dreht man die Spritze auf den Kopf, drückt die überschüssige
Luft heraus und verschließt die Spitze mit Hilfe eines Feuerzeugs
luftdicht.
Durchführung:
Die Lösung
in der Spritze hat anfangs eine gelbe Färbung. Wenn man die
Spritze nun auseinander zieht und die Lösung schüttelt,
verfärbt sich die Lösung grün/blau. Um den Effekt
der Farbänderung aufrecht zu halten, muss entweder die Spritze
auf Spannung gehalten werden (was aber ziemlich viel Kraft erfordert)
oder man fixiert die aufgezogene Spritze mit zwei 1 Cent Münzen
(siehe Bilder)
Sobald das ursprüngliche Volumen in der Spritze wieder hergestellt
wird, färbt sich die Lösung wieder gelblich.
Dieser Vorgang ist reversibel und kann unbegrenzt wiederholt werden.
|
|
| |
 Versuchsverlauf
in Bildern:
Versuchsverlauf
in Bildern: |
|
|
|
Vor
Zugabe des Indikators |
Zugabe
von Trockeneis |
Ausgasen
von CO2 |
|
|
 |
ohne
CO2 |
mit
CO2 |
|
|
Abschmelzen
der Spritze |
Stabilisierung
der aufgezogenen Spritze |
|
|
| |
Entsorgung:
(siehe auch Entsorgungsmaßnahmen)
Die Lösung enthält keine gefährlichen
Chemikalien. Sie kann über den Ausguss entsorgt werden.
|
|
| |
Erklärung
/ Hintergrund:
Bei Reaktionen mit Gasen kann Druck die Lage des Gleichgewichts
beeinflussen. Wenn man festes Trockeneis in Wasser wirft, sublimiert
es sofort, d.h. es wird gasförmig und löst sich z.T. im
Wasser. Ein Teil des Gases entweicht sofort als große Blasen
aus dem System.
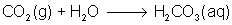
Der Indikator
färbt sich zu Beginn gelb, weil sich Kohlendioxid in
Wasser löst und somit Kohlensäure entsteht. Übt
man nun einen Unterdruck auf das System aus, indem man die
Spritze auseinander zieht, dann entweicht das Kohlendioxid
gasförmig aus der Lösung; es weicht dem äußeren
Zwang aus.
Die
Lösung wird neutral, was durch die grüne Farbe
des Indikators, nachdem die Lösung geschüttelt
wurde, sichtbar wird.
Wenn man genau
hinsieht, erkennt man beim Auseinanderziehen kleine Bläschen
(CO2) aus der Lösung aufsteigen bzw. ausgasen
(siehe Bild).
|
|
Durch
erneutes Zusammendrücken der Spritze, kann man das CO2
wieder in Lösung bringen und die Lösung wird wieder gelb.
|
|
| |
Links:
Die
Indikator-Schulwebseite : Alles Rund um chemische Farb-Indikatoren.
Wie sind sie aufgebaut? Wann wirken sie? Welche pH-Bereiche gibt
es? Auf diese und viele weitere Fragen gibt die Seite von Prof.
Blumes Bildungsserver für Chemie ausführliche Antworten.
Rotkohlsaft
als Indikator: Mit einfachen Mitteln wird gezeigt wie man aus
zerkleinerten Rotkohlblätter sich einen Universalindikator
herstellt.
Säure-Base-Indikatoren:
Sie werden verwendet um bei Titrationen abhängig vom pH-Wert
der Lösung einen Farbumschlag anzuzeigen.
Trockeneis:
Informationen über Trockeneis
Versuch
Nr.46: Magnesium, ein faszinierendes Metall (Teil II: Reaktion
mit Trockeneis)
Vielen
Dank an Nani, Ini und Karo (Uni Würzburg). |
|
|