| |
|
|
| |
Gummibärchen im flammenden Inferno |
|
|
|
|
| |
Versuch
Nr.011
Bewertung / Schwierigkeitsgrad:   
Zeitaufwand: 15 Minuten |
|
|
| 
|
| |
|
|
| |
Ziel:
Man wirft ein normales Gummibärchen in eine Kaliumchlorat-Schmelze.
Ein helles Glühen sowie ein lautes Brummen setzt ein und löst
das Bärchen in einer spektakulären Reaktion auf.
|
|
| |
Geräte:
Großes Reagenzglas, Stativ mit Klemme, Schüssel
mit Löschsand, Bunsenbrenner, Schutzscheibe, Schutzbrille,
Schutzhandschuhe
|
|
| |
Chemikalien:
15g Kaliumchlorat, Gummibärchen
|
|
| |
Sicherheitshinweise:
Achtung: Die Reaktion muss hinter einem Schutzschild in einem Abzug
erfolgen!
In der Nähe des Versuchs dürfen sich keine brennbaren
Stoffe befinden, und die Unterlage muss feuerfest sein. Kaluimchlorat
ist ein sehr starkes Oxidationsmittel; die meisten organischen Stoffe
werden unter Feuererscheinung oder explosionsartig zersetzt.
Kaliumchlorat (KClO3):
O,Xn R9-20/22 S13-16-27
Gummibärchen (???): keine Gefahr beim Verschlucken :-)
 O O
 Xn Xn
|
|
| |
Einverständniserklärung:
Hiermit erklären Sie sich bereit den folgenden Versuch unter
eigener Verantwortung
und nur mit ausreichendem chemischen Wissen und geeigneten Schutzvorrichtungen
durchzuführen!
Der Autor kann für jegliche Personen- und Sachschäden
durch mögliche Fehlversuche nicht haftbar gemacht werden. (siehe
Sicherheitscheck bzw. Disclaimer) |
|
| |
|
|
| |
Versuchsanleitung: 
15g Kaliumchlorat werden mit einem Bunsenbrenner in einem
großen Reagenzglas vorsichtig(!) geschmolzen. Anschließend
lässt man ein Gummibärchen in die Kaliumchloratschmelze
fallen. Die Reaktion beginnt sofort. Das Gummibärchen verbrennt
unter intensivem Aufglühen, tanzt auf der Salzschmelze und
erzeugt ein merkliches Geräusch (Brummen,Rauschen!)
Vorsicht: Häufig ist die Reaktion so heftig, dass ein
Teil des Kaliumchlorats mit dem entstehenden Kohlendioxid und Wasser
hinausgeschleudert wird. Daher sollte das Reagenzglas leicht schräg
eingespannt und nicht auf die Beobachter gerichtet werden!
|
|
| |
Entsorgung:
(siehe auch Entsorgungsmaßnahmen)
Kaliumchlorat wird mit Salzsäure verkocht und anschließend
mit einer Base (NaOH) neutralisiert. Das neutralisierte Produkt
kann in den Abguß geschüttet werden.
|
|
| |
Erklärung
/ Hintergrund:
Es ist anzunehmen, dass beim Versuch mit dem Gummibärchen bei
der Temperatur des geschmolzenen Kaliumchlorats, Wasser aus der
Gummibärchenmasse freigesetzt wird und mit dem Kaliumchlorat
zu Chlorsäure reagiert. Diese leitet dann die Verbrennung der
Zucker (Saccharose, Glucose, Fructose) im Gummibärchen ein.
Desweiteren
disproportioniert Kaliumchlorat ab 400°C zu Kaliumchlorid und
Kaliumperchlorat, welches dann selbst sehr rasch in Sauerstoff und
Kaliumchlorid zerfällt.
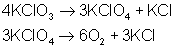
Dabei
wird die Gelantine im Gummibärchen unter Feuererscheinung zu
CO2 und Wasser oxidiert. Das Brummen und Rauschen entsteht
durch die bei der Verbrennung entstehenden Gase, die das Bärchen
immer wieder mit sich reißen.
|
|
| |
Sonstiges:
Die Sicherheitsvorkehrungen müssen unbedingt beachtet werden!
Mit dem Versuch lässt sich sehr anschaulich demonstrieren,
dass Chlorsäure-Gemische leicht oxidierbarer Stoffe (hier eine
Saccharose-Kaliumchlorat-Mischung) spotan zur Entzündung und
zu einer beeindruckenden exothermen Reaktion gebracht werden können.
|
|
| |
Links:
Gummibaeren-Forschung.de
Tiefe Einblicke in die Welt der Gummibärchen ;-)
Haribo.de
die Erschaffer des süßesten Bären der Welt
Rezept
für Gummibärchen: jetzt kann sich jeder selbst seine
eigenen Bärchen machen
Kaliumchlorat:
Eigenschaften, Herstellung, Verwendung
Sauerstoffhaltige
Säuren des Chlors: Herstellung, Strukturen und Eigenschaften
(Uni Bayreuth)
Betriebsanweisung
Kaliumchlorat: von der Uni Würzburg
|
|